 |
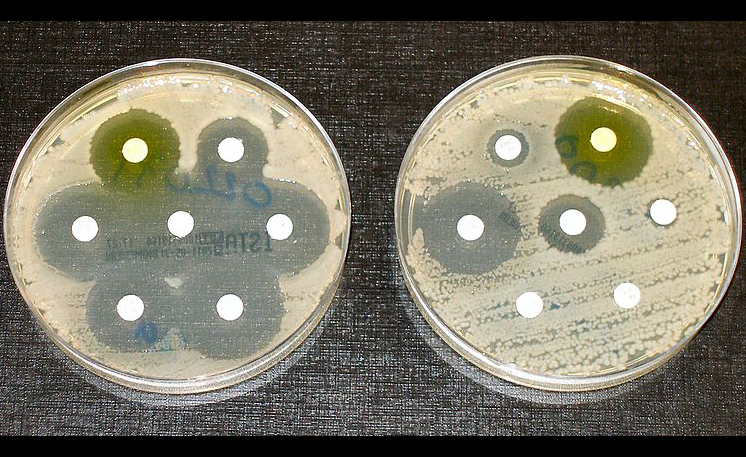
| Antybiotykooporność widoczna na hodowli bakterii. Autor: dr Graham Beards, Wikimedia |
Antybiotyki, bakterie i antybiotykooporność
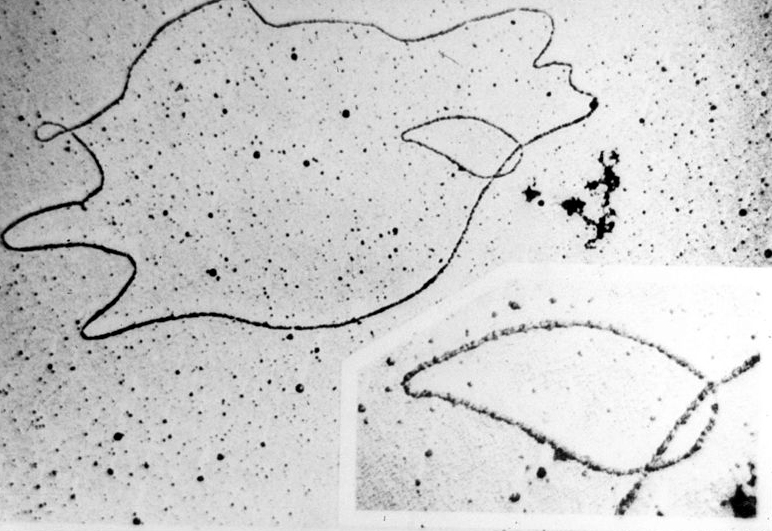 |
| Mikrografia elektronowa chromosomu bakteryjnego (większa pętla) i plazmidu (mniejsza pętla). Za: National Institute of Health |
Antybiotykooporność – mechanizmy ochrony bakterii
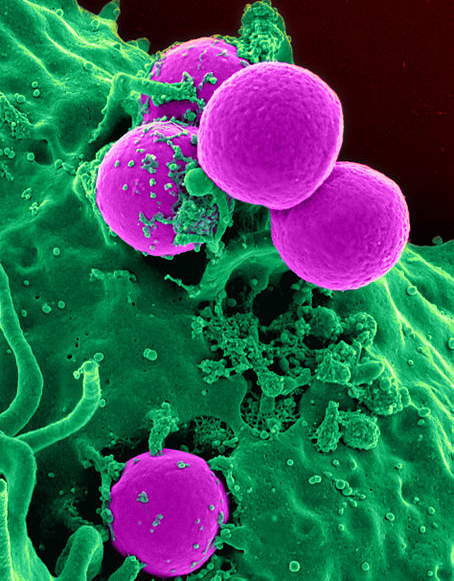 |
| Mikrografia elektronowa (koloryzowana) neutrofila ludzkiego fagocytującego gronkowca MRSA. Za: National Institute of Health |
Oporność na antybiotyki – z czego wynika?
 |
| Alexander Fleming. Za: Calibuon, English Wikibooks |
Oporność na antybiotyki: przeciwdziałanie i poszukiwanie rozwiązań
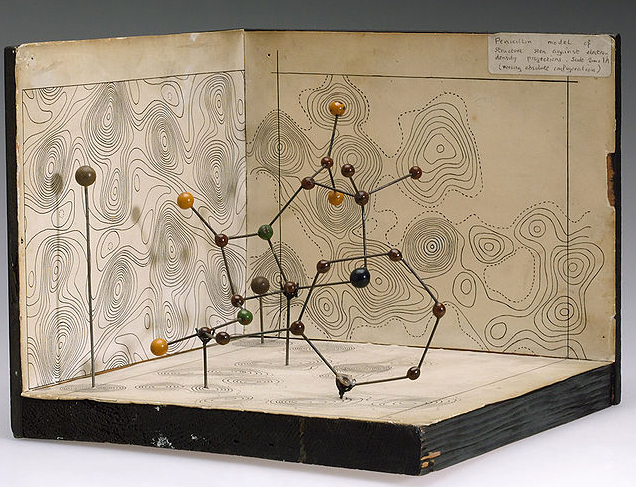 |
| Budowa chemiczna penicyliny. Model Dorothy Hodgkin, noblistki w dziedzinie chemii. Za: Science Museum London, Science and Society Picture Library |
Programy ochrony antybiotyków przeciwko antybiotykooporności
 |
|
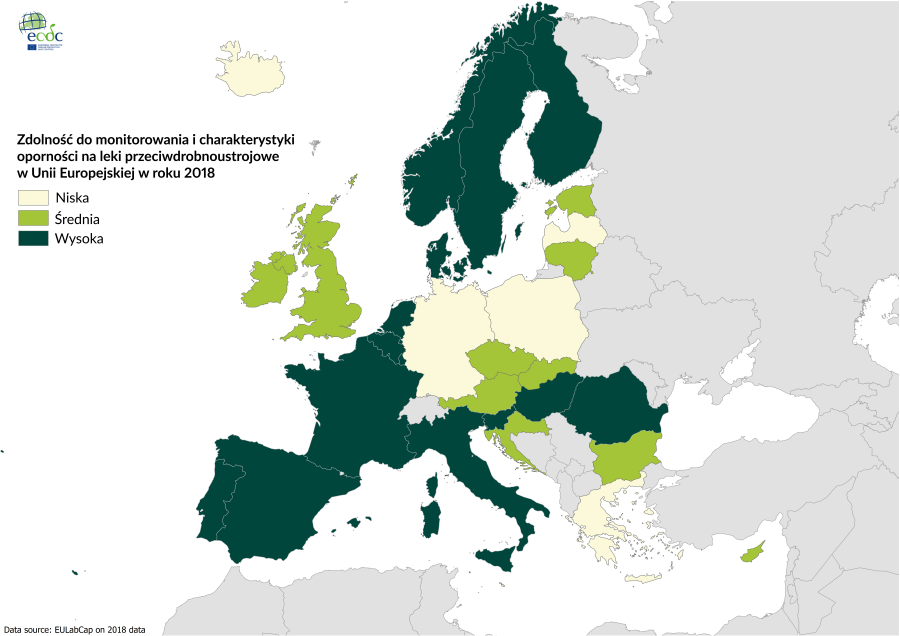
Jakość monitoringu oporności na antybiotyki w Unii Europejskiej.
Za: Europejskie Centrum ds. Zapobiegania i Kontroli Chorób (ECDC), z późn. zm.
|
Nowe antybiotyki i inne środki przeciwbakteryjne (bakteriofagi)
 |
| Antybiotyki. Za: Grzegorz Skibka, Pixabay |
Sztuczna inteligencja w pomocy przy poszukiwaniu nowych antybiotyków
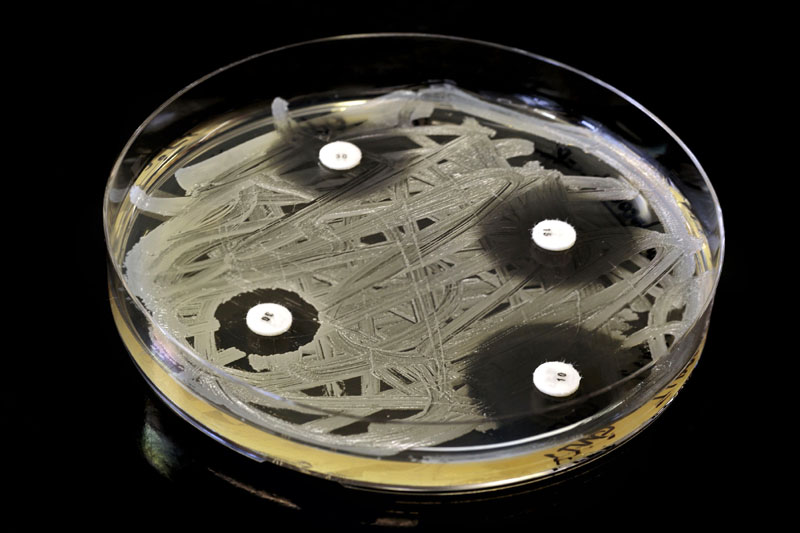 |
| Badanie wrażliwości na antybiotyk i widoczna rosnąca antybiotykooporność. Za: Peqsels |
Polscy naukowcy badają antybiotykooporność i antybiotyki
Literatura: antybiotykooporność
https://uniwersyteckie.pl/nauka/prof-mariusz-jaskolski-wojna-z-antybiotykoopornoscia
https://www.medpagetoday.com/InfectiousDisease/GeneralInfectiousDisease/24708
https://www.nik.gov.pl/aktualnosci/antybiotyki-i-co-dalej.html
Jadwiga Baj. „Mikrobiologia”. Wydawnictwo Naukowe PWN. Warszawa 2018.
Kim, Seungsoo, Tami D. Lieberman, and Roy Kishony. „Alternating antibiotic treatments constrain evolutionary paths to multidrug resistance.” Proceedings of the National Academy of Sciences (2014).
Raczynska, Joanna E., et al. „A close look onto structural models and primary ligands of metallo-β-lactamases.” Drug Resistance Updates (2018).
Stokes, Jonathan M., et al. „A deep learning approach to antibiotic discovery.” Cell (2020).












Pierwsze zatajone przypadki zakażenia koronawirusem w Chinach, były już w połowie listopada. W grudniu informowali o tym lekarze, a także niezależni blogerzy w internecie. Jednym z lekarzy, który pierwszy poinforował o koronawirusie był lekarz Li Wenliang. Za to partia komunistyczna, aresztowała lekarza i poddała go torturom – aby zaprzeczył istnieniu koronawirusa. 30 Stycznia bohaterski lekarz Li Wenliang umiera, właśnie na koronawirusa. W swoim testamecie przytacza słowa św. Pawła, "W dobrych zawodach wystąpiłem, bieg ukończyłem, wiary ustrzegłem." 2 List do Tymoteusza 4, 7-8
Petycja o ukaranie komunistycznych Chin, za ukrywanie prawdy o koronawirusie. https://tiny.pl/tbb4g
Dzięki!
Bardzo ważną przyczyną oporności na antybiotyki jest także nadużywanie ich w hodowli zwierząt tzw. "hodowlanych". Dlaczego nic o tym nie ma? Artykuł poza tym bardzo dobry ale pominięcie tak ważnej kwestii to duży błąd.
Super wpis, wiele istotnych informacji i dobrze opisane 🙂
Technologii żywności (zamiast technologii żywienia) 😀